Elektrolyse und Brennstoffzelle: Enzym ersetzt Platin als Katalysator
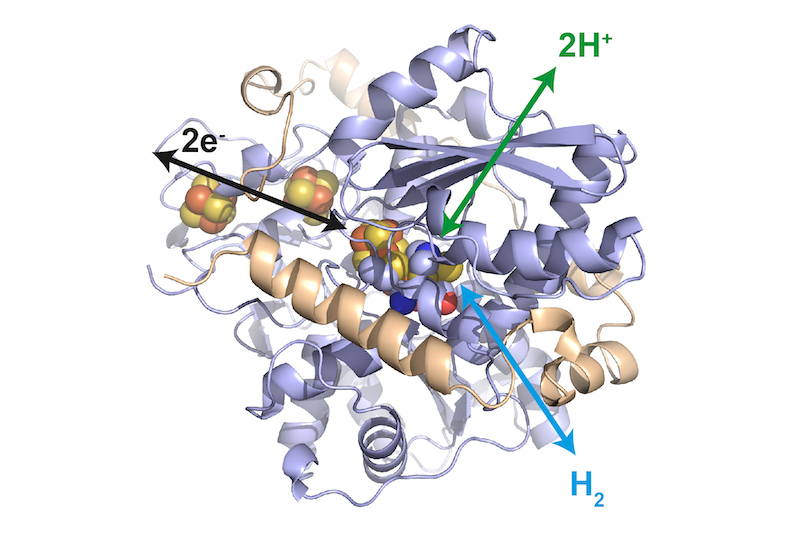 Dr. James Birrell / MPI CEC
Dr. James Birrell / MPI CEC Ein Enzym könnte als Biokatalysator in Elektrolyseuren und Brennstoffzellen dienen und so das teure Platin als Katalysator ersetzen. Biokatalysatoren galten bisher als zu instabil, da sie stark mit Sauerstoff reagieren. Um das Enzym zu schützen, ist es für den Einsatz in der Brennstoffzelle oder dem Elektrolyseur daher in ein Polymer eingebettet. So soll es nicht nur im Labor, sondern auch technisch nutzbar werden. Ein Team der Technischen Universität München (TUM) der Ruhr-Universität Bochum, des CNRS Marseille und des Max-Planck-Instituts für Chemische Energiekonversion in Mülheim an der Ruhr hat das System im Wissenschaftsjournal Nature Catalysis vorgestellt.
Spezielle Enzyme mit Potenzial für die Wasserstoffwirtschaft, sogenannte Hydrogenasen, sind bereits lange bekannt. Sie katalysieren die Umwandlung von Wasserstoff sehr schnell und nahezu ohne Energieverlust.
Haltbarkeit vs. Wirkungsgrad
„Bettet man die empfindlichen Hydrogenasen in geeignete Polymere ein, so arbeiten sie auch in Gegenwart von Sauerstoff mehrere Wochen“, sagt Nicolas Plumeré, Professor für Elektrobiotechnologie am TUM Campus Straubing für Biotechnologie und Nachhaltigkeit. „Ohne diesen Schutz verlieren sie ihre Aktivität innerhalb von Minuten.“
Auch die Idee des Einbettens in sogenannte Redox-Polymere ist nicht neu. Dabei handelt es sich um Kunststoffe, deren Moleküle Seitengruppen haben, die Elektronen übertragen können. Doch selbst diese Spezialkunststoffe stellten bisher eine zu große Barriere für den Elektronenfluss dar. Um diese zu überwinden, geht viel Energie in Form von Wärme verloren. Die Fähigkeit, Wasserstoff zu erzeugen, büßten die eingebetteten Hydrogenasen dabei sogar ganz ein.
Durch geschickte Auswahl und Kombination der Polymer-Seitengruppen gelang es dem Forschungsteam, das Redoxpotenzial des Polymers so einzustellen, dass sich der Widerstand schon mit einer geringen Überspannung überwinden lässt. In einem weiteren Schritt erreichten sie, dass die Hydrogenase den Prozess in beide Richtungen katalysiert.
Enzym-Brennstoffzelle zeigt gute Leistung
Mit diesem System baute das Forschungsteam das Enzym in eine Biologische Brennstoffzelle ein. Das Enzym Bilirubin-Oxidase reduziert dabei Sauerstoff aus dem Bakterium Myrothecium verrucaria. Die im Polymerfilm eingebettete Hydrogenase oxidiert Wasserstoff aus dem Bakterium Desulfovibrio desulfuricans und erzeugt dabei Strom.
Die Brennstoffzelle erreicht eine Leerlaufspannung von 1,16 Volt. Das sei der höchste jemals für ein solches System gemessene Wert und liege nahe am thermodynamischen Maximum, heißt es von der TUM. Die Stromdichte der Zelle lag bei drei Milliampere pro Quadratzentimeter – laut TUM ist dieser Wert für biologische Zellen sehr hoch.
Auch für die umgekehrte Reaktion, die Wasserstoffproduktion durch Aufnahme von Elektronen, ist das System einsetzbar: Seine Effizienz bei der Energieumwandlung liegt auch bei Stromdichten von über vier Milliampere pro Quadratzentimeter nahe 100 Prozent.
Blaupause für neue Biokatalysatoren
„Die Verringerung des Energieverlusts hat zwei entscheidende Vorteile“, sagt Nicolas Plumeré. „Das System wird dadurch nicht nur wesentlich effizienter. Bei hohen Leistungen wäre die in einem Brennstoffzellen-Stack entstehende Wärme für die biologischen Systeme ein Problem.“
Bevor die Bio-Brennstoffzelle Systemen auf Platinbasis Konkurrenz macht, muss die Stabilität der Hydrogenasen bei hohen Stromdichten noch steigen. Das will das Team in den nächsten Schritten erreichen.
Zudem könnten die Erkenntnisse auch auf andere hochaktive aber empfindliche Katalysatoren übertragen werden. Ein nahe liegendes Ziel: Enzyme, die aus Kohlendioxid mit Hilfe von Strom direkt flüssige Brennstoffe oder Zwischenstufen für deren Erzeugung gewinnen.
Biologische Abläufe für den Einsatz in der Energiewende werden auch in anderen Fachgebieten untersucht, zum Beispiel für die organische Photovoltaik oder die Bioenergie. Im großen Stil sind sie aber vor allem beim Biogas im Einsatz. Hier gibt es sogar eine “Mikrobe des Jahres”.
14.5.2021 | Quelle: TUM | solarserver.de © Solarthemen Media GmbH.com